Controversias del manejo de la pancreatitis aguda en el servicio de emergencias. Bolaños-Valverde M. y cols. ISSN 2215-5562. Rev. Ter. Julio-Diciembre del 2025; Vol.19 N°2:63-78.
ARTÍCULO DE REVISIÓN
Controversias del manejo de la pancreatitis aguda en el servicio de emergencias: una revisión literaria actualizada
Controversies in the management of acute pancreatitis in the emergency department: An updated literature review
Título corto: Controversias del manejo de la pancreatitis aguda en el servicio de emergencias.
Autor: 1María Laura Bolaños-Valverde, 1Cristian Coto-Arias, 1Rodrigo Torres-Rojas, 1Paula Batallas-Arguedas, 2,3 Wilfredo E. Gómez-Herrera.
Filiación: 1 Médico General independiente, San José, Costa Rica. 2 Hospital México, Caja Costarricense de Seguro Social, San José, Costa Rica. 3Programa Estudios de Posgrado en Medicina de Emergencias, Universidad de Costa Rica, San José, Costa Rica.
Correspondencia: Wilfredo E. Gómez-Herrera, correo electrónico: wgomez@resusimtation.com
Financiamiento: ninguno.
Conflictos de Interés: ninguno.
Forma de citar: Bolaños-Valverde ML, Coto-Arias C, Torres-Rojas R, Batallas-Arguedas P, Gómez-Herrera WE. Controversias del manejo de la pancreatitis aguda en el servicio de emergencias: una revisión literaria actualizada. Rev Ter[Internet]. 2025;19(2): 63-78.
Rev. Ter. Julio-Diciembre del 2025; Vol. 19 N°2
Fecha de envío: 30 de junio del 2025.
Fecha de aceptación: 7 de julio del 2025.
Abreviaturas: ACS, síndrome compartimental abdominal; AGA, Asociación Americana de Gastroenterología; AGC, Colegio Americano en Gastroenterología; BUN, nitrógeno ureico sanguíneo; CPRE, colangiopancreatografía retrógrada endoscópica; ECAs, ensayos clínicos aleatorizados; FC, frecuencia cardíaca; FR, frecuencia respiratoria; Hto, hematocrito; NE, nutrición enteral; NG, nasogástrica; NP, nutrición parenteral; NRS, riesgo nutricional; NY, nasoyeyunal; PA, pancreatitis aguda; PAM, presión arterial media; PCR, proteína C-reactiva; PCT, procalcitonina; PVC, presión venosa central; SEM, Servicio de Emergencias; SIRS, síndrome de respuesta inflamatoria sistémica; VCI, vena cava inferior.
Resumen
Objetivo: identificar las estrategias de manejo controversiales de la pancreatitis aguda en el servicio de emergencias y literatura que las apoya o las rechaza. Metodología: se realizó un estudio de revisión sistemática de la literatura de tipo cualitativo narrativo que evalúa la eficacia y seguridad de diversas estrategias en el manejo de la pancreatitis aguda en el servicio de emergencias. Se buscaron artículos publicados entre 2018 y 2025, en bases de datos reconocidas como PubMed, Cochrane, Database of Systematic Reviews, Google Scholar, Web of Science y Scopus, tanto en español como inglés. Resultados: se incluyeron un total de 28 artículos científicos que incluían abordajes como hidratación intravenosa agresiva, nutrición temprana y vías de alimentación, uso profiláctico de antibióticos, intervenciones invasivas como colangiopancreatografía retrógrada endoscópica y drenajes percutáneos, abdominales o quirúrgicos. Se examinaron sus asociaciones con complicaciones, duración de la estancia hospitalaria, morbilidad, mortalidad y severidad de la enfermedad, proporcionando un marco actualizado para la toma de decisiones clínicas en este contexto. Conclusiones: se recomienda el uso de fluidoterapia con metas medibles (“goal-directed”) versus hidratación agresiva. La nutrición vía oral se debe de comenzar lo antes posible a tolerancia del paciente. De considerarse clínicamente, se prefiere sonda nasogástrica sobre nasoyeyunal, con algunas excepciones. Nutrición parenteral se reserva como último recurso o como soporte en caso de no conseguir las metas nutricionales. La antibioticoterapia se debe de utilizar solo en casos exclusivos donde se confirme o exista sospecha clínica fuerte que existe un proceso infeccioso, y no rutinariamente de forma profiláctica. La CPRE urgente se recomienda solo en casos donde exista colangitis o colelitiasis persistente concomitantemente. Las intervenciones más invasivas deben de tener un enfoque escalonado, agotar tratamientos no invasivos y valoraciones multidisciplinarias.
Palabras clave: pancreatitis aguda, tratamiento, hidratación, antibioticoterapia, nutrición, CPRE, servicio de emergencias.
Abstract
Objective: Identify controversial management strategies for acute pancreatitis in the context of an emergency department and the literature that supports or rejects them. Methodology: A qualitative narrative systematic literature review was conducted to evaluate the efficacy and safety of various strategies in the management of acute pancreatitis in the emergency department. Articles published between 2018 and 2025 were searched in recognized databases such as PubMed, Cochrane, Database of Systematic Reviews, Google Scholar, Web of Science and Scopus, both in Spanish and English. Results: A total of 28 scientific articles were included, covering approaches such as aggressive intravenous hydration, early nutrition and feeding routes, prophylactic antibiotic use, invasive interventions such as endoscopic retrograde cholangiopancreatography, and percutaneous, abdominal, or surgical drainage. Their associations with complications, length of hospital stay, morbidity, mortality, and disease severity were examined, providing an updated framework for clinical decision-making in this setting. Conclusions: The use of goal-directed fluid therapy is recommended versus aggressive hydration. Oral nutrition should be started as soon as possible, depending on the patient's tolerance. If clinically indicated, a nasogastric tube is preferred over a naso-jejunal tube, with some exceptions. Parenteral nutrition is reserved as a last resort or as a backup if nutritional goals are not achieved. Antibiotic therapy should be used only in select cases where an infectious process is confirmed or strongly suspected, and not routinely as a prophylactic measure. Urgent ERCP is recommended only in cases with concomitant persistent cholangitis or cholelithiasis. More invasive interventions should be stepwise, exhausting noninvasive treatments and involving multidisciplinary assessments.
Keywords: acute pancreatitis, treatment, hydration, antibiotic therapy, nutrition, ERCP, emergency department.
Introducción
La pancreatitis aguda (PA) es una de las consultas más comunes en el Servicio de Emergencias (SEM) con una incidencia estimada de 34 personas por cada 100 000 al año a nivel mundial1. En estos servicios, la PA constituye una causa frecuente de consulta por dolor abdominal agudo2.
Se caracteriza por un dolor local y una respuesta sistémica inflamatoria con un curso clínico variable según la severidad de la presentación. La mayoría de los pacientes tienen un curso leve autolimitado que tiende a resolver durante los siguientes 8 días1,2. Sin embargo, un porcentaje menor tiende a desarrollar un curso clínico moderado o severo con una mortalidad que puede alcanzar entre el 15 y 20%, especialmente en pacientes con complicaciones como infección, necrosis o falla multiorgánica persistente3,4.
El manejo de la PA ha evolucionado considerablemente en los últimos 10 años en donde se destaca un abordaje multidisciplinario con intervenciones más efectivas que reducen tanto la morbilidad como la mortalidad1,2, así como el obtener un diagnóstico temprano a través de métodos más efectivos, determinando la causa y por ende un tratamiento certero más preciso. Sin embargo, existen diversas estrategias terapéuticas cuyo uso se puede considerar controversial.
El presente artículo revisará estrategias del manejo de la pancreatitis aguda consideradas controvertidas en el SEM y que han evolucionado debido a su correlación con mortalidad, morbilidad y el desenlace de la enfermedad. Se analizará la literatura científica que respalda o rechaza estrategias como la hidratación intravenosa agresiva, nutrición temprana, uso profiláctico de antibioticoterapia e intervenciones invasivas con el objetivo de ofrecer una visión crítica y actualizada que permita optimizar la atención y mejorar el pronóstico de los pacientes con pancreatitis aguda atendidos en los servicios de emergencias.
Metodología
Se realizó un estudio de revisión sistemática de la literatura de tipo cualitativo que responde a la interrogante ¿cuáles son las estrategias del manejo de la pancreatitis aguda consideradas controvertidas en el SEM? El diseño y desarrollo de esta investigación toma como base los criterios que estipula Preferred Reporting Items for Systematic Reviews and Meta-Analyses (PRISMA) 5. Se realizó una búsqueda de artículos publicados entre 2018 y 2025, que cumplieran los criterios de inclusión: revisiones sistemáticas, metaanálisis, ensayos clínicos, guías clínicas, revisiones de casos y revisiones narrativas, que aborden estrategias de manejo, protocolos o tratamientos de pancreatitis aguda. Se incluyeron publicaciones en bases de datos reconocidas como PubMed, Cochrane, Database of Systematic Reviews, Google Scholar, Web of Science y Scopus, tanto en español como inglés.
Para la búsqueda se utilizó los siguientes términos de búsqueda: (("pancreatitis aguda"[Title/Abstract] OR "acute pancreatitis"[Title/Abstract]) AND ("manejo"[Title/Abstract] OR "protocolo"[Title/Abstract] OR "tratamiento"[Title/Abstract])) AND (("systematic review"[Publication Type] OR "meta-analysis"[Publication Type] OR "review"[Publication Type] OR "expert opinion"[Title/Abstract])) AND ("2018/01/01"[Date - Publication] : "2025/03/31"[Date - Publication]) y ("acute pancreatitis" OR "pancreatitis aguda") AND (management OR protocol OR treatment).
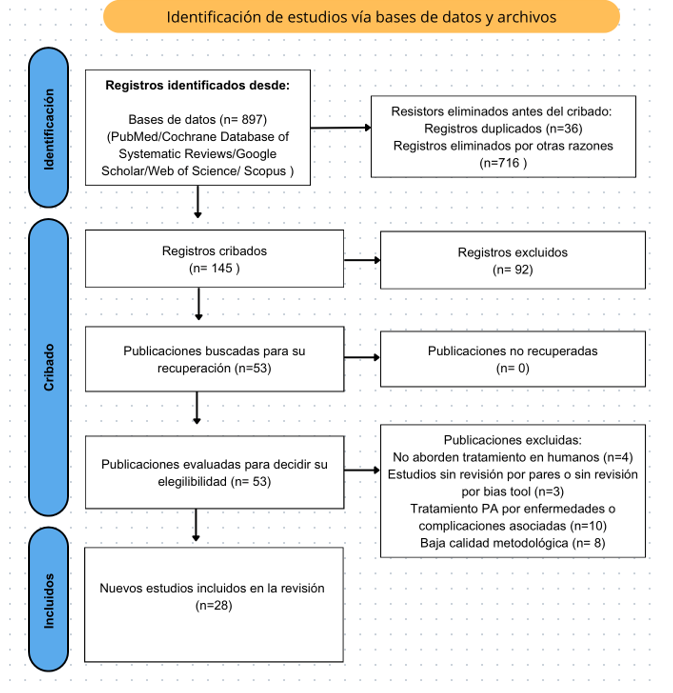
Esta estrategia arrojó un total de 897 artículos. Se excluyeron aquellos artículos que no fuesen dentro del plazo establecido de años conformando 145. Posteriormente se valoró que no fuesen estudios que se centren en protocolos específicos con limitaciones regionales o institucionales que dificulten su generalización, artículos que no aborden directamente el manejo o tratamiento de pancreatitis aguda en humanos, publicaciones fuera del rango temporal establecido, o estudios sin revisión por pares o sin revisión por bias tool, dando un total de 53 artículos. Posteriormente se analizaron los artículos que abordaran tratamiento directamente sin otras enfermedades asociadas o complicaciones y los duplicados, llegando a 36 artículos. Finalmente, 8 artículos fueron descartados por baja calidad metodológica, llevando a un total de 28 artículos utilizados (ver Figura 1).
Resultados y Discusión
Debido a que la salud del paciente puede verse afectada por periodos de estancia prolongada en los servicios de salud, complicaciones asociadas, aumento en mortalidad y comorbilidad de acuerdo con el abordaje que se realice, es de suma importancia optimizar la atención en los SEM con evidencia actualizada y científica, específicamente abordando los temas controversiales. La tabla 1 resumen las características de los artículos incluidos en la revisión.

Figura1. Flujograma de PRISMA para identificación y selección de los artículos incluidos.
Fuente: elaboración propia, según PRISMA 20205.
Tabla 1. Artículos incluidos en la revisión sistemática
|
Autor y número de referencia |
Revista / Año |
Tipo de Estudio |
Conclusiones |
|
|
|
|
|
|
Boxhoorn et al 1 |
Lancet, 2020 |
Revisión sistemática |
Tratamiento inicial: reanimación con fluidoterapia dirigida según predictores de sobrecarga hídrica, deshidratación y estabilidad hemodinámica. Soporte nutricional enteral primeras 24 a 72 horas. CPRE en pancreatitis biliar aguda únicamente en concomitancia con colangitis, considerar si existe persistencia de colestasis. Antibioticoterapia solo en infecciones secundarias, no se recomienda profilácticamente. |
|
Leppäniemi et al 2 |
World J Emerg Surg, 2019 |
Guía clínica WSES |
Guía clínica basada en evidencia por consenso internacional en el manejo de la pancreatitis aguda severa. La PCR es el gold standard para definir severidad y riesgo de complicaciones. PCT de 3.8ng/ml o mayor dentro de las primeras 96 horas de inicio de síntomas tiene una sensibilidad y especificidad del 93% y 79% para predecir necrosis pancreática. Antibioticoterapia profiláctica no tiene una diferencia significativa en disminuir mortalidad o morbilidad, no se recomienda para todo paciente con PA. Antes de realizar descompresión intraabdominal se debe de considerar sedación profunda, parálisis inducida o drenaje percutáneo. Nutrición enteral es preferida sobre parenteral. CPRE no está indicada en pancreatitis biliar, solo en pacientes con colangitis u obstrucción del conducto biliar común. |
|
Garro-Urbina3 |
Revista Médica Sinergia, 2020 |
Revisión narrativa |
Manejo escalonado con técnicas mínimamente invasivas; uso prudente de antibióticos; importancia de colecistectomía en pancreatitis biliar. |
|
Rodríguez Revelo et al 4 |
RECIMUNDO, 2020 |
Revisión narrativa |
Tratamiento individualizado; nutrición enteral y parenteral total. Manejo con soporte y Antibióticos solo en casos indicados con uso inadecuado que resulta en evolución desfavorable. Importancia del equipo multidisciplinario. Hidratación agresiva como parte pilar del tratamiento. Abordaje quirúrgico y endoscópico en casos limitados. |
|
Page et al5 |
Rev Esp Cardiol, 2020 |
Guía |
Guía actualizada para publicación. Declaración PRISMA |
|
Oland et al6 |
HepatoBiliary Surg Nutr., 2022 |
Revisión narrativa |
No recomiendan la reanimación con fluidoterapia de 3-5mL/kg/h durante las primeras 24 horas. Nutrición enteral es recomendada sobre la parenteral al reducir mortalidad, infección sistémica y posiblemente infección local. No se recomienda la colocación sistemática de sonda naso-yeyunal sobre la nasogástrica. CPRE se recomienda en PA con colangitis concomitante. No se recomienda el uso de antibioticoterapia profiláctica. Se recomienda la monitorización continua de la presión intraabdominal en las primeras 72 horas si invasivamente ventilado. |
|
Crockett. et al 7 |
Gastroenterology, 2018 |
Guía clínica (AGA) |
Recomiendan “goal directed” para la fluidoterapia. Nutrición enteral oral temprana (dentro de las primeras 24hrs) a tolerancia. Si intolerancia a la vía oral, se recomienda nutrición por sonda enteral versus parenteral. Si PA biliar, colecistectomía durante la admisión inicial y no posponerla. |
|
Tenner et al.8 |
Am J Gastroenterol, 2024 |
Guía clínica (ACG) |
Reanimación intravenosa moderada dirigida a objetivos clínicos para evitar sobrecarga hídrica. Bolos adicionales si evidencia de hipovolemia. Solución de Lactato de Ringer sobre solución salina. Revaloración cada 6 horas en las primeras 24 a 48 horas con la meta de reducir BUN. Nutrición enteral temprana vía oral (24-72hrs) a tolerancia del paciente y si hemo dinámicamente estable. Vía enteral preferida sobre la parenteral. Uso de sonda nasogástrica sobre naso-yeyunal. No utilizar antibioticoterapia profiláctica en PA sin evidencia clara de infección. CPRE urgente indicada solo en pacientes con pancreatitis biliar aguda con colangitis concomitante o colestasis persistente realizada en las primeras 24 horas. |
|
Szatmary et al 9 |
Drugs |
Revisión narrativa |
Diagnóstico y tratamiento actualizados; énfasis en manejo temprano y prevención de complicaciones; revisión de guías clínicas. |
|
Valverde-López et al10 |
Medicina clínica |
Revisión narrativa |
Descripción clínica, diagnóstico y tratamiento; énfasis en manejo integral y prevención de recurrencias. Fluidoterapia basado en metas. Nutrición enteral precoz. Antibioticoterapia indicada en casos específicos, no como profilaxis. |
|
Yaowmaneerat et al 11 |
World J Gastrointest Pharmacol Ther. 2023 |
Revisión narrativa |
Fluidoterapia es pilar en tratamiento agudo. Fluidoterapia agresiva se asocia a aumento en mortalidad y efectos adversos severos. Lactato de Ringer es superior a las soluciones salinas. Manejo por metas. Hto puede guiar el ajuste de la fluidoterapia con una meta de <44%. |
|
Gomes et al12 |
Ann R Coll Surg Engl, 2020 |
Revisión narrativa |
Primer paso de perfusión en la PA es alcanzar una presión venosa central de 12-15mmHg, gasto urinario de 0.5-1ml/kg/h y un índice de colapsabilidad de la VCI >48%. Nutrición enteral precoz gástrica o post-pilórica. Nutrición parenteral en casos donde la meta calórica no se alcanza. CPRE cuando se asocia colangitis, curso clínico impredecible o ictericia ascendente. Manejo de colecciones pancreáticas o necrosis. Antibióticos cuando se documenta infección. Cirugía representa 3 D’s (“delay, drain, debride”). Se prefiere el método mínimamente invasivo con abordaje por pasos gradualmente hacia procedimientos más invasivos cuando el tratamiento previo falla. |
|
Dawson et al 13 |
HPB (Oxford), 2023 |
Revisión sistemática y metaanálisis |
Reanimación intravenosa moderada es recomendado en el manejo inicial de la PA. No hay diferencia significativa en mortalidad entre solución salina o Lactato de Ringer. Tratados con solución salina sí presentaron mayor estancia hospitalaria. |
|
Costea et al 14 |
Diagnostics, 2025 |
Revisión sistemática |
Cristaloides como Lactato de Ringer son superiores a la solución salina reduciendo SIRS, falla orgánica, y estancia en UCI, sin diferencia significativa en mortalidad. Reanimación con fluidoterapia moderada es superior a la agresiva. |
|
Takada et al. 15 |
J. Hepatobiliary Pancreat Sci. 2022 |
Guía clínica (Japón) |
Nutrición enteral temprana, incluyendo pequeñas porciones. Fluidoterapia agresiva con monitorización continua para evitar sobrecarga hídrica en especial en adultos mayores, insuficiencia cardiaca o lesión renal con evidencia muy pobre. Si se utiliza infusión con cristaloides, se debe de utilizar solución salina como buffer con evidencia baja. Antibioticoterapia profiláctica no es recomendada. Colecistectomía temprana para PA por colelitiasis. Hipertensión intraabdominal >20mmHg (síndrome compartimental abdominal). Se debe monitorizar la presión intraabdominal en casos de fluidoterapia masiva, enfermedad severa, enfermedad renal concomitante o falla respiratoria. |
|
Guilabert et al 16 |
Gastroenterol Clin N Am, 2025 |
Revisión narrativa |
Manejo inicial con reanimación con fluidoterapia moderada y “goal directed” es preferida sobre agresiva. Antibióticos y antifúngicos solo cuando se sospecha necrosis pancreática infectada u otras infecciones concomitantes y no profiláctico. Nutrición enteral temprana. |
|
Ma et al17 |
Front Pharmacol, 2022 |
Revisión de casos |
Infusión de albúmina en pacientes hospitalizados no muestra una diferencia estadísticamente significativa en pronóstico y se asocia a mayor estancia hospitalaria y UCI. |
|
Ramírez-Maldonado et al 18 |
Ann Surg, 2021 |
Ensayo Clínico aleatorizado |
Del 2017 al 2019, en 4 hospitales, 2 grupos de tratamiento: realimentación oral inmediata (dieta sólida baja en grasa inmediatamente a la admisión hospitalaria) y alimentación oral convencional (progresiva con la mejoría de laboratorios y clínica). 130 pacientes incluidos. La dieta con sólidos baja en grasa inmediata es segura y posible en PA leve y moderada, costo efectiva y sin causar efectos adversos o complicaciones. |
|
Mederos et al19 |
JAMA, 2021 |
Revisión sistemática |
Fluidoterapia para reanimación iniciada inmediatamente con soluciones cristaloides preferiblemente, Lactato de Ringer, titulando respecto a metas medibles de perfusión. La nutrición enteral de inicio temprano entre las 24 y 72 horas, si no toleran VO utilizar vía nasoenteral y si contraindicaciones o complicaciones vía parenteral. Utilizar NRS para tamizaje nutricional. |
|
Gopi et al20 |
JGS, 2023 |
Revisión Narrativa |
Nutrición enteral oral es la ruta preferida, sin embargo, en casos específicos se sugiere la vía nasoenteral o parenteral, en especial en casos de inestabilidad hemodinámica. No hay suficiente evidencia para definir si de forma intermitente o continua. |
|
Lakananurak et al21 |
World J Clin Cases, 2020 |
Revisión narrativa |
Nutrición medida con IC como gold standars, sino meta calórica de 25kcal/kg/día con proteína requerida estimada en adultos sanos de 1.2-1.5g/kg/día. Nutrición enteral es preferida sobre otras vías. Naso-yeyunal considerada en casos donde no se tolere vía oral o nasogástrica. Nutrición enteral cuando intolerancia a vía enteral por complicaciones severas. |
|
Arvanitakis et al22 |
Clin Nutr, 2024 |
Guía práctica clínica ESPEN |
Nutrición VO iniciada al momento de tolerancia e independientemente del nivel de lipasa sérica con PA leve. Baja en grasa es la dieta recomendada. Nutrición enteral preferida sobre parenteral inicio temprano entre las 24 y 72hrs de admisión y en casos de intolerancia VO. Dieta estandarizada polimérica es la recomendada. Vía nasogástrica sobre la naso yeyunal, excepto en casos de intolerancia digestiva. Si presión intraabdominal (PIA) >15 mmHg la vía recomendada es naso-yeyunal a 20mL/h e incrementando de acuerdo con tolerancia. Si PIA >20 mmHg o con síndrome compartimental abdominal, nutrición enteral debe de temporalmente detenerse e iniciar parenteral suplementado con glutamina. No se recomiendan enzimas pancreáticas a menos de casos obvios de insuficiencia pancreática exocrina. |
|
Wang et al 23 |
BMC Gastroenterol, 2024 |
Revisión sistemática y metaanálisis |
Nutrición vía nasogástrica iniciada a las 48hrs de admisión incrementa riesgo de diarreas e infección, pero no impacta significativamente la mortalidad o necesidad de intervención quirúrgica. |
|
Dutta et al 24 |
Cochrane Database Syst Rev., 2020 |
Revisión sistemática |
Comparación entre 5 ECAs, total de 220 participantes adultos de India, Escocia y EEUU. No hay diferencia significativa entre nutrición enteral nasogástrica versus naso-yeyunal con respecto a la mortalidad. No encontraron suficiente evidencia para concluir superioridad, inferioridad o equivalencia entre ambos modos de nutrición enteral por sonda en pacientes con PA aguda. |
|
Badia et al 25 |
Antibiotics (Basel), 2024 |
Revisión narrativa |
Tratamiento preventivo (profiláctico) con antibioticoterapia (ATB) no disminuye mortalidad o necrosis pancreática infectada y más bien puede asociarse a un aumento de riesgo de infecciones fúngicas. El diagnóstico temprano o sospecha clínica de infección por necrosis pancreática puede basarse en niveles de PCT y otros métodos microbiológicos más novedosos, y no solo por TAC o cultivos. Cuando indicado, el inicio temprano de ATB es determinante para reducir mortalidad. ATB con buena penetrancia pancreática debe de ser utilizado. La duración de la terapia debe de mantenerse al mínimo y basado en condición del paciente. |
|
Severino et al 26 |
Antibiotics (Basel), 2023 |
Revisión narrativa |
El uso de antibióticos de forma preventiva en la PA se ha asociado a resistencia microbiana y efectos adversos. El uso debe de ser exclusivo de ciertos casos y se debe considerar el perfil microbiológico, penetrancia y patrones de resistencia local. Se recomienda una terapia combinada de amplio espectro que cubra bacterias Gram negativas y Gram positivas. |
|
Schepers et al27 |
Lancet, 2020 |
Ensayo clínico aleatorizado |
Ensayo aleatorizado, multicéntrico, paralelo, en 1, 2017, 232 pacientes con PA biliar grave predicha sin colangitis comparando el uso de CPRE con esfinterotomía dentro de las primeras 24 horas versus tratamiento conservador. No se encontró reducción significativa de mortalidad o complicaciones mayores. Concluyen que la CPRE urgente solamente sea indicada en casos con colangitis concomitante o colelitiasis persistente. |
|
Bansal et al 28 |
World J Clin Cases, 2022 |
Revisión narrativa |
Indicación para drenaje percutáneo en PA es necrosis infectada en la fase temprana con una mejoría del 50% de los pacientes. Se recomienda actualmente esperar 3 a 4 semanas desde inicio de la enfermedad para realizarlo. También indicado en casos donde el manejo no invasivo por sí solo no es suficiente. Se ha visto mejoría en pacientes con presión intraabdominal aumentada el uso de paracentesis abdominal para drenaje. |
Fuente: Elaboración propia de los autores basado en Boxhoom et al 1, Leppäniemi et al 2, Garro-Urbina et al 3 , Rodríguez Revelo et al 4 , Page et al 5, Oland et al6, Crockett et al7, Tenner et al8, Swatmary et al9, Valverde-López et al10, Yaowmaneerat et al11, Gomes et al12, Dawson et al13, Costea et al14, Takada et al15, Guilabert et al16, Ma et al17, Ramírez- Maldonado et al18, Mederos et al19, Gopi et al20, Lakananurak et al21, Arvanitakis et al22, Wang et al23, Dutta et al24, Badia et al25,Severino et al26, Schepers et al27, Bansal et al28.
Hidratación agresiva
El manejo de la pancreatitis aguda en el SEM incluye la reanimación con líquidos intravenosos como pilar fundamental para mantener la perfusión tisular, prevenir la progresión a falla orgánica y corregir la hipovolemia causada por la depleción del volumen intravascular y la inflamación pancreática1,4. Tradicionalmente, la hidratación agresiva con grandes volúmenes (5-10 mL/kg/h) ha sido recomendada para prevenir complicaciones como el síndrome de respuesta inflamatoria sistémica (SIRS) y la falla orgánica. Sin embargo, estudios recientes y guías internacionales6, como la Asociación Americana de Gastroenterología (AGA)7 y el Colegio Americano en Gastroenterología (ACG)8 sugieren que esta estrategia puede aumentar el riesgo de sobrecarga de volumen, edema pulmonar y complicaciones hemodinámicas, especialmente en pacientes con otras comorbilidades.
Para la adecuada reanimación con fluidoterapia, lo autores como Szatmary et al9 y Valverde-López et al10 proponen la monitorización continua de signos vitales, con metas (frecuencia cardiaca (FC) <120 lpm, frecuencia respiratoria (FR) <22 rpm, PAM >65 mmHg), parámetros clínicos como el gasto urinario (>0,5 mL/kg/h) y de laboratorios como el nitrógeno ureico sanguíneo (BUN, por sus siglas en inglés) y el hematocrito (Hto), y que este último se mantenga en entre 35% y 44% para identificar hemoconcentración o hemodilución, ya que una hemoconcentración persistente durante 24 horas, se ha asociado al desarrollo de pancreatitis necrotizante y falla orgánica. Además, recomiendan no dejarse llevar por parámetros normales ya que el cuadro clínico tiende a evolucionar dentro de las 36 horas siguientes4. Por otro lado, mediciones del estado del volumen intravascular y presión intraabdominal, son herramientas fundamentales para ajustar la terapia de fluidos de manera individualizada, especialmente en pacientes con comorbilidades que aumentan el riesgo de complicaciones por exceso de líquidos2,4,6,8. Con ello, se busca alcanzar objetivos clínicos específicos e individualizados, que además sean medibles.
Para estimar la volemia se pueden acudir a métodos como la presión venosa central (PVC) o ecografía de la vena cava inferior (VCI), así como la medición de la presión intraabdominal es útil para detectar hipertensión intraabdominal precoz, ya que la PA tiende a causar filtración intravascular hacia el peritoneo con una tasa promedio de 2 a 4 L en las primeras 48 horas4. Se recomienda, por lo tanto, mantener la PVC en un rango permisivo de 8 a 12 mmHg, lo que permite un equilibrio entre la corrección de la hipovolemia y la prevención de la sobrecarga de volumen, en especial en pancreatitis moderada a severa12,13. Por otro lado, la ecografía de la VCI es una herramienta no invasiva valiosa para evaluar el estado de volumen intravascular. Un índice de colapsabilidad respiratoria de la VCI superior al 40-50% sugiere hipovolemia y explora la probabilidad de una adecuada respuesta a la administración de fluidos, mientras que valores menores apuntan a normovolemia o sobrecarga hídrica4,12.
En cuanto a la administración de líquidos intravenosos, varios autores 10-14 recomiendan iniciar con hidratación moderada (1,5mL/kg/h a 5-10mL/kg/h) tan pronto se diagnostique la pancreatitis aguda, llegando a un consenso de una ventana terapéutica más reducida y periodo crítico para la resucitación temprana de 4-6 horas desde la llegada al hospital. Un artículo de Yaowmaneerat et al11, menciona que en un estudio multicéntrico mostró que administrar más de 1 litro en las primeras 4 horas reduce significativamente la necesidad de intervenciones comparado con menos de 0,5 litros. Además, el artículo11 menciona que la que en las primeras 48 horas, el secuestro de fluidos se estima de 3,7 L en pancreatitis leve y 5,6 L en pancreatitis severa. Es importante recalcar que según el paciente, hay factores que predicen mayor necesidad de fluidos como lo sería la edad (jóvenes > adultos), el Hto >45%, la glucemia al azar >160mg/dL, síndrome de respuesta inflamatoria sistémica (SIRS) ≥ 2, y aquellos con historia de consumo excesivo de alcohol, debido a que indican mayor secuestro y necesidad de resucitación más agresiva11,14. Mientras que la ACG8 recomienda 250-500 mL/h en las primeras 12-24 h, la guía Japonesa15 recomienda 150-600 mL/h en pacientes con shock o hipovolemia, y de 130-150 mL/h en otros pacientes. Otros autores a partir de múltiples revisiones sistemáticas y metaanálisis sugieren resucitación dirigida a objetivos (“goal-directed”), con tasas iniciales de desde 1,5mL/kg/h hasta alcanzar metas clínicas6,9,11,16. Varios ensayos clínicos aleatorizados (ECAs) confirmaron que la hidratación agresiva (10-15 mL/kg/h) no aporta beneficios y que puede ser dañina asociando un aumento en mortalidad y complicaciones (fallo respiratorio, ACS, sepsis) comparado con tasas más bajas (5-10 mL/kg/h). Debido a que la evidencia es moderada y baja, por lo que se requieren más estudios para definir el volumen y la velocidad óptimos de infusión1,9-14.
Multiples autores6-8,11-14 recomiendan que la hidratación se realice preferiblemente con soluciones cristaloides isotónicas como lactato de Ringer, debido a su efecto de atenuar la respuesta inflamatoria y menor riesgo de SIRS a las 72 hrs en comparación con solución salina, aunque la evidencia aún es de calidad moderada a baja. Se destaca dentro de los artículos, que el uso de coloides debería de limitarse debido a que la evidencia ha demostrado que no disminuyen la mortalidad e inclusive se ha visto asociado a un riesgo aumentado de falla orgánica11,13,14,16.
En cuanto al uso de infusiones de albúmina, no existe suficiente evidencia que respalde su uso debido a que no se ha logrado establecer su beneficio indiferentemente de los niveles de albúmina iniciales, infección o cantidad de infusión administrada. Sin embargo, en una revisión sistemática17, menciona que el uso de albúmina diluida en dextrán redujo la mortalidad hasta un 7,7%, sin mencionar la severidad de la pancreatitis, así como una meta terapéutica de albúmina en suero de 3,7-4g/dL, para mejorar pronóstico a mediano plazo.
Desde la perspectiva clínica, la controversia entre hidratación agresiva y moderada radica en equilibrar la necesidad de restaurar la perfusión tisular y prevenir la progresión de la pancreatitis severa, con el riesgo de complicaciones derivadas de la sobrecarga hídrica. Mientras algunos expertos defienden la reanimación agresiva temprana para reducir la mortalidad y la morbilidad, otros advierten sobre los efectos adversos de esta práctica, especialmente en pacientes con insuficiencia renal o cardíaca. Por ello, el manejo actual tiende a individualizar la terapia de fluidos, evitando protocolos rígidos. Por lo tanto, se busca lograr un protocolo de reanimación dirigida a metas (“goal-directed fluid therapy”), ajustando la velocidad y volumen de líquidos según objetivos clínicos y parámetros medibles, en especial en las primeras 24 horas1,3,8,12,16.
Nutrición temprana
La nutrición y la ingesta calórica son aspectos críticos en el manejo de la PA, ya que el balance energético influye directamente en la necesidad de terapia con líquidos y en la homeostasis metabólica. En pacientes críticamente enfermos, una ingesta calórica insuficiente puede causar catabolismo, pérdida muscular y balance hídrico negativo, aumentando la necesidad de fluidos agresivamente para mantener la estabilidad hemodinámica; sin embargo, se debe evitar la sobrealimentación, ya que puede exacerbar la inflamación sistémica18,19.
Por esto se recomienda20,21 medir el gasto energético en reposo idealmente con la calorimetría indirecta, pero al no ser accesible en muchos centros o situaciones, se recomienda el uso de ecuaciones predictivas como la de Harris-Benedict, Tamizaje de Riesgo Nutricional (NRS, por sus siglas en inglés) o Riesgo Nutricional en Críticos (NUTRIC score, por sus siglas en inglés)20. Las guías actuales sugieren un objetivo energético de 25-30kcal/kg/día en pacientes críticos, sin embargo, es importante tomar en cuenta el gasto energético medido, y actualizarlo conforme se avanza con el paciente4,9,14,16,21.
En cuanto a la vía de administración, algunos autores19,21 concuerdan con la preferencia de una nutrición enteral (NE) sobre la nutrición parenteral (NP) para preservar la integridad intestinal, reducir riesgo de infecciones ya que previene la translocación bacteriana y mejora evolución clínica. Esta se debe de iniciar lo antes posible en cuanto el paciente tolere, idealmente dentro de las primeras 24 horas cuando la PA es leve, inclusive moderada10,19. La NP se puede iniciar desde el ingreso en pacientes desnutridos, con factores predictivos de pancreatitis grave, hipertensión intraabdominal, íleo paralítico, obstrucción, o que se hayan complicado con NE y aquellos quienes dentro de las 72 horas no cubran al menos el 60% de sus requerimientos por vía oral19,21.
En los estudios más recientes se ha visto una mejoría de la evolución del paciente, con recuperación más rápida cuando se inicia una dieta oral temprana, generalmente dentro de las 24 a 72 horas19-21, indiferentemente de la concentración sérica de lipasa en pacientes con PA leve22. Su inicio depende de la tolerancia clínica del paciente y la estabilidad hemodinámica. No se basa en un solo marcador, sino en una evaluación clínica integral que incluye: ausencia de dolor abdominal intenso o progresivo que impida la ingesta; ausencia de náuseas o vómitos persistentes; estabilidad hemodinámica con tendencia a la mejoría de marcadores inflamatorios y metabólicos, incluyendo, pero no limitado a, la mejoría de la severidad con la evaluación con escalas como Ranson o APACHE II; y la capacidad para tolerar la ingesta oral sin complicaciones (distensión abdominal o intolerancia). Se recalca que no se requiere iniciar con líquidos claros; se puede comenzar con dieta blanda o sólida baja en grasa, favoreciendo la recuperación más rápida y evitando el ayuno prolongado19,21.
Previamente, se consideraba que una dieta yeyunal podría reducir la estimulación pancreática y por ende disminuir la posibilidad de que sus enzimas aumentaran el proceso de auto digestión18. Sin embargo, en una revisión sistemática y metaanálisis23 se observó que la alimentación vía nasogástrica (NG) versus la nasoyeyunal (NY), no tenían diferencias estadísticamente significativas en cuanto a términos de metas energéticas o mortalidad, sin embargo, sí se encontró un aumento de riesgo de infección y diarrea con la sonda NG. Dutta et al24 mencionan que no existe suficiente evidencia para concluir diferencias entre ambas vías de administración en pacientes con pancreatitis severa.
No obstante, se debe considerar que la sonda NG es un procedimiento con menos complicaciones, bajo costo y más accesible que la sonda NY24, y se ha considerado por varios autores8,16,18,20,22 como la primera línea de tratamiento en pacientes con pancreatitis severa. Por otro lado, la sonda NY, se puede considerar para aquellos pacientes que indiferentemente de la severidad de la pancreatitis, presenten una gastroparesia severa, dolor, nauseas persistentes u obstrucción parcial de la salida gástrica por complicaciones de la PA (edema, o pseudoquiste), ya que así evita el transito gástrico comprometido, sin intervenir en la administración directa de nutrientes18,19,21,22.
En los pacientes con PA que requieren vasopresores, la NE debe iniciarse tan pronto como la estabilidad hemodinámica lo permita. Gopi et al20 mencionan un ECA en el que se utilizó la estrategia de una alimentación reducida con un 40-60% de las calorías estimadas, en pacientes críticamente enfermos, mostrando que esto no afecta negativamente la mortalidad, infecciones ni la duración de la hospitalización, siempre que se logre mantener una ingesta adecuada de proteínas (1,2-1,5g/kg/día). Con lo anterior también se recomienda evaluar continuamente la perfusión intestinal y monitorizar signos de intolerancia digestiva (distensión o íleo). Es importante recalcar que en pacientes con inestabilidad hemodinámica que requieren de dosis altas de vasopresores o fluctuantes, isquemia intestinal, íleo severo o síndrome compartimental abdominal (ACS, por sus siglas en inglés), la NE está contraindicada y se puede buscar optimizar el soporte nutricional por medio de NP22. Sin embargo, en pacientes que están con NP, que no se contraindique la vía enteral y que no presenten fístulas, la alimentación con pequeños volúmenes para estimular el intestino sin cubrir las necesidades calóricas completas, se puede utilizar con el fin de preservar la función intestinal, prevenir la atrofia de mucosas y mejorar la barrera intestinal20,21.
En cuanto a la suplementación de la nutrición, las enzimas pancreáticas se deberían de utilizar en los casos donde exista una insuficiencia pancreática exocrina clara o malabsorción con esteatorrea, ya que no existe suficiente evidencia que respalde el uso general de las mismas22. Por otro lado, el tipo de dieta que los autores20,22 recomiendan es la polimérica estandarizada en NE para PA indiferentemente de la severidad, con un grado de recomendación alto. Finalmente, la alimentación vía enteral de forma continua se sigue utilizando debido a que de forma intermitente se ha asociado a diarreas20 y no se encontró evidencia clínica sustentable que la apoye.
Antibioticoterapia profiláctica
La PA, en su mayoría, se presenta como una afección estéril, por lo que el uso profiláctico de antibióticos no está recomendado en ningún grado de severidad8,9,16. Según Rodríguez Revelo et al4, el empleo de antibióticos debe reservarse exclusivamente para casos con sospecha confirmada de infección pancreática o extra-pancreática, particularmente cuando existe deterioro clínico o falta de mejoría con el tratamiento estándar. La selección del antibiótico debe basarse en la sensibilidad del microorganismo identificado, dentro de los cuales se debe considerar bacterias Gram negativas (en especial Escherichia coli, Klebsiella spp. y Pseudomonas aeruginosa), Gram positivas (Enterococcus faecium, Enterococcus faecalis, Estafilococo epidermidis, Estafilococo aureus) y fúngicas (Candida spp.), sin olvidar que estos pacientes pueden encontrarse en riesgo, según su condición, de organismos multi drogo resistentes (MDROs)6,25. Además, la duración del tratamiento debe ajustarse según la respuesta clínica del paciente y los resultados en los cultivos microbiológicos2,25.
En cuanto a la influencia del uso de antibióticos en la mortalidad y morbilidad, no existe evidencia que demuestre que la profilaxis antibiótica reduzca estos desenlaces en pacientes con PA,10. Por el contrario, el uso innecesario puede incrementar el riesgo de efectos adversos10 como infecciones fúngicas intraabdominales, favorecer la resistencia bacteriana, e inclusive complicar el manejo clínico. La necesidad real de antibióticos se recomienda1,2,8,9,12,25 únicamente cuando se confirma o se sospecha clínicamente una infección secundaria como la presencia de deterioro clínico progresivo, ausencia de mejoría con el tratamiento convencional, necrosis infecciosa y/o cultivos positivos que identifiquen el patógeno causante de la infección.
Es importante recalcar que se puede valorar el inicio de uso de antibióticos cuando, además de signos clínicos, se obtengan laboratorios con una proteína C reactiva (PCR)2,9 específicamente un incremento de más de 90mg/dL desde el ingreso o por encima de 190mg/dL después de 48 horas ya que puede predecir el nivel de severidad, así como niveles de procalcitonina (PCT) elevados2,25 debido a que estos han sido útiles en predecir el desarrollo de una necrosis pancreática y por ende cuáles pacientes se podrían beneficiar de un uso temprano de antibióticos6,26. Varios estudios mencionados por Severino et al26 utilizaron niveles séricos seriados de PCT para el inicio, continuación o finalización del uso de antibióticos, lo que resultó en dosis más bajas del mismo sin un impacto negativo en el resultado de la PA.
Intervenciones invasivas en contexto agudo
El uso de intervenciones invasivas no es rutinariamente requerido en la PA, con excepción de algunos escenarios como lo sería la PA con colangitis aguda, con o sin evidencia de obstrucción biliar, donde se recomienda2,3,4,6-8, una colangiopancreatografía retrógrada endoscópica (CPRE) urgente dentro de las primeras 24 a 72 horas. Un ECA27 demostró que en pacientes con PA biliar severa, pero sin colangitis, la realización urgente de CPRE con esfinterotomía no reduce significativamente las complicaciones mayores ni la mortalidad en comparación con tratamiento conservador, por lo que recomiendan su uso en pacientes con colangitis o colestasis persistente.
Por otro lado, cuando se presenta la PA con otras complicaciones asociadas como lo sería el ACS con presiones abdominales >20mmHg4,28, necrosis infectada con signos claros de deterioro clínico6, hemorragias o fístulas28, es decir, escenarios que no mejoran con el manejo conservador y aumentan significativamente la mortalidad del paciente, se debe requerir valoración para drenaje percutáneo o descompresión quirúrgica6,28. La AGA7, refiere que el drenaje percutáneo se debe considerar en pacientes con colecciones infecciosas o necrotizantes de forma temprana en el periodo agudo. Sin embargo, el artículo de Bansal et al28, mencionan un enfoque escalonado, donde se aplazan las intervenciones a más de 3 semanas desde su inicio, lo que permite la encapsulación de la colección, llevando a un tejido necrótico más definido, evitando una futura insuficiencia pancreática y mejorando la morbilidad. También mencionan que un drenaje por paracentesis abdominal previo al drenaje percutáneo para disminuir la presión intraabdominal en PA moderada o severa, puede mejorar la gravedad clínica, acortar la estancia hospitalaria y reducir la mortalidad, sin repercutir en complicaciones infecciosas.
Conclusiones
La hidratación debe ser suficiente para corregir la hipovolemia sin inducir complicaciones, y la decisión debe basarse en la evaluación continua del paciente y la evidencia clínica disponible con base a determinantes hemodinámicos medibles, evitando los protocolos rígidos. Es recomendado globalmente el inicio de la nutrición enteral lo antes posible, idealmente dentro de las primeras 24 a 72 horas. Sin embargo, en pacientes con intolerancia, contraindicaciones o inestabilidad hemodinámica, la alimentación parenteral o en pequeñas cantidades, son alternativas para preservar la función intestinal, mantener los requerimientos calóricos, evitar complicaciones y mejorar el pronóstico del paciente.
El uso de antibióticos profilácticos en la PA no está recomendado, ya que no reduce mortalidad ni morbilidad. Se reservan para casos con infección confirmada o alta sospecha clínica, usando marcadores como la procalcitonina para guiar su uso. Por otro lado, las intervenciones invasivas en un contexto de urgencia, como CPRE o drenajes percutáneos o quirúrgicos, se reservan para escenarios específicos basándose en indicaciones claras para mejorar la supervivencia del paciente. Se recomienda el abordaje escalonado, con metas medibles y objetivas, y terapias dirigidas sin regímenes estrictos, con el fin de reducir la morbilidad y mortalidad de los pacientes con PA.
Referencias bibliográficas
1. Boxhoorn L, Voermans RP, Bouwense SA, Bruno MJ, Verdonk RC, Boermeester MA, et al. Acute pancreatitis. Lancet [Internet]. 2020;396(10252):726–34. doi: 10.1016/S0140-6736(20)31310-6
2. Leppäniemi A, Tolonen M, Tarasconi A, Segovia-Lohse H, Gamberini E, Kirkpatrick AW, et al. 2019 WSES guidelines for the management of severe acute pancreatitis. World J Emerg Surg [Internet]. 2019;14(1):27. doi: 10.1186/s13017-019-0247-0
3. Garro Urbina V, Thuel Gutiérrez M. Diagnóstico y tratamiento de pancreatitis aguda. Rev Medica Sinerg [Internet]. 2020;5(7):e537. doi: 10.31434/rms.v5i7.537
4. Rodríguez Revelo ME, Yánez Piedra PA, Zapata Paredes PR, Novoa Obregón AE. Recomendaciones en el manejo actual de la pancreatitis aguda. Recimundo [Internet]. 2020;4(2):86-93. doi: 10.26820/recimundo/4.(2).mayo.2020.86-93
5. Page MJ, McKenzie JE, Bossuyt PM, Boutron I, Hoffmann TC, Mulrow CD, et al. Declaración PRISMA 2020: una guía actualizada para la publicación de revisiones sistemáticas. Rev Esp Cardiol [Internet]. 2021;74(9):790–799. doi: 10.1016/j.recesp.2021.06.016
6. Oland GL, Hines OJ.New guidelines for the treatment of severe acute pancreatitis. Hepatobiliary Surg Nutr[Internet]. 2022; 11(6):913-916. doi: 10.21037/hbsn-22-532
7. Crockett SD, Wani S, Gardner TB, Falck-Ytter Y, Barkun AN, American Gastroenterological Association Institute Clinical Guidelines Committee. American gastroenterological association institute guideline on initial management of acute pancreatitis. Gastroenterol [Internet]. 2018;154(4):1096–1101. doi: 10.1053/j.gastro.2018.01.032
8. Tenner S, Vege SS, Sheth SG, Sauer B, Yang A, Conwell DL, et al. American college of gastroenterology guidelines: Management of acute pancreatitis. Am J Gastroenterol [Internet]. 2024;119(3):419–437. doi: 10.14309/ajg.0000000000002645
9. Szatmary P, Grammatikopoulos T, Wenhao C, Huang W, Mukherjee R, Halloran C et al. Acute pancreatitis: Diagnosis an treatment.. Drugs [Internet]. 2022; 82(12): 1251-1176. doi: 10.1007/s40265-022-01766-4
10. Valverde-López F, Martínez-Cara JG, Redondo-Cerezo E. Acute pancreatitis Med clin[Internet]. 2022;158(11): 556-563. doi: 10.1016/j.medcle.2021.12.006
11. Yaowmaneerat T, Sirinawasatien A. Update on the strategy for intravenous fluid treatment in acute pancreatitis. World J Gastrointest Pharmacol Ther [Internet]. 2023 ;14(3):22-32. doi: 10.4292/wjgpt.v14.i3.22
12. Gomes CA, Di Saverio S, Sartelli M, Segallini E, Cilloni N, Pezzilli R, et al. Severe acute pancreatitis: eight fundamental steps revised according to the “PANCREAS” acronym. Ann R Coll Surg Engl [Internet]. 2020;102(8):555–599. doi: 10.1308/rcsann.2020.0029
13. Dawson A, Karunakaran M, Sharma ZD, Ullah S, Barreto SG. Fluid resuscitation in the early management of acute pancreatitis - evidence from a systematic review and meta-analysis. HPB (Oxford) [Internet]. 2023;25(12):1451–1465. doi: 10.1016/j.hpb.2023.08.013
14. Costea CN, Pojoga C, Seicean A. Advances in the Management of Fluid Resuscitation in Acute Pancreatitis: A Systematic Review. Diagnostics [Internet]. 2025; 15(7): 810. doi: 10.3390/diagnostics15070810
15. Takada T, Isaji S, Mayumi T, Yoshida M, Takeyama Y, Itoi T, et al. JPM clinical practice guidelines 2021 with easy-to-understand explanations for the management of acute pancreatitis. J Hepatobiliary Pancreat Sci [Internet]. 2022; 29(10):1057-1083.
16. Guilabert L, Cárdenas-Jaén, de-Madaria E. Initial Management of Acute Pancreatitis. Gastroenterol Clin N Am [Internet]. 2025; 54(1):21-36. doi: 10.1016/j.gtc.2024.07.001
17. Ma Y, Yan T, Xu F, Ding J, Yang B, Ma Q, Wu Z, Lyu J, Wang Z. Infusion of Human Albumin on Acute Pancreatitis Therapy: New Tricks for Old Dog? Front Pharmacol [Internet]. 2022;13:842108. doi: 10.3389/fphar.2022.842108
18. Ramírez-Maldonado E, López Gordo S, Pueyo EM, Sánchez-García A, Mayol S, González, et al. Immediate Oral Refeeding in Patients With Mild and Moderate Acute Pancreatitis: A Multicenter, Randomized Controlled Trial (PADI trial). Ann Surg [Internet]. 2021;274(2):255-263. doi: 10.1097/SLA.0000000000004596
19. Mederos MA, Reber HA, Girgis MD. Acute Pancreatitis: A Review. JAMA. 2021;325(4): 382-390. doi:10.1001/jama.2020.20317
20. Gopi S, Saraya A, Gunjan D. Nutrition in acute pancreatitis.World J Gastrointest Surg [Internet]. 2023;15(4):534-543. doi: 10.4240/wjgs.v15.i4.534
21. Lakananurak N, Gramlich L. Nutrition management in acute pancreatitis: Clinical practice consideration. World J Clin Cases [Internet]. 2020;8(9): 1561-1573. doi: 10.12998/wjcc.v8.i9.1561.
22. Arvanitakis M, Ockenga J, Bezmarevic M, Gianotti L, Krznaric Ž, Lobo DN, et al. ESPEN practical guideline on clinical nutrition in acute and chronic pancreatitis. Clin Nutr [Internet]. 2024;43(2):395–412. doi: 10.1016/j.clnu.2023.12.019
23. Wang M, Shi H, Chen Q, Su B, Dong X, Shi H, Xu S. Comparative safety assessment of nasogastric versus nasojejunal feeding initiated within 48 hours post-admission versus unrestricted timing in moderate or severe acute pancreatitis: a systematic review and meta-analysis. BMC Gastroenterol [Internet]. 2024;24(1):207. doi: 10.1186/s12876-024-03290-z
24. Dutta AK, Goel A, Kirubakaran R, Chacko A, Tharyan P. Nasogastric versus nasojejunal tube feeding for severe acute pancreatitis. Cochrane Database Syst Rev. [Internet]. 2020;3(3):CD010582. doi: 10.1002/14651858.CD010582.pub2
25. Badia JM, Amador S, González-Sánchez C, Rubio-Pérez I, Manuel-Vázquez A, Juvany M, et al. Appropriate use of antibiotics in acute pancreatitis: A scoping review. Antibiotics [Internet]. 2024;13(9). doi: 10.3390/antibiotics13090894
26. Severino A, Varca S, Airola C, Mezza T, Gasbarrini A, Franceschi F, et al. Antibiotic Utilization in Acute Pancreatitis: A Narrative Review. Antibiotics [Internet]. 2023;12(7):1120. doi: 10.3390/antibiotics12071120
27. Schepers NJ, Hallensleben NDL, Besselink MG, Anten MPGF, Bollen TL, Da Costa DW, et al. Urgent endoscopic retrograde cholangiopancreatography with sphincterotomy versus conservative treatment in predicted severe acute gallstone pancreatitis (APEC): a multicentre randomised controlled trial. Lancet [Internet]. 2020;396(10245):167–176. doi: 10.1016/S0140-6736(20)30539-0
28. Bansal A, Gupta P, Singh AK, Shah J, Samanta J, Mandavdhare HS, et al. Drainage of pancreatic fluid collections in acute pancreatitis: A comprehensive overview. World J Clin Cases[Internet]. 2022;10(20):6769-6783. doi: 10.12998/wjcc.v10.i20.6769